Une nouvelle variante de l’édition génomique, appelée « Prime Editing », est très médiatisée depuis sa publication dans la revue spécialisée Nature fin octobre 2019. Même si le Prime Editing n’en est qu’à ses débuts, la presse le présente déjà comme une méthode révolutionnaire qui devrait transformer le génie génétique et la médecine et permettre de traiter par thérapie génique plus de 80 % des maladies héréditaires jusqu’ici incurables, telles que la drépanocytose. Il pourrait également être utilisé pour le développement de variétés. Sa précision accrue est particulièrement appréciée. Ce qui frappe, c’est que les ciseaux génétiques CRISPR/Cas9, jusqu’alors présentés comme extrêmement précis, sont soudainement montrés sous un mauvais jour. Au lieu d’être considérés comme un outil chirurgical de précision, ils sont désormais plutôt présentés comme des ciseaux de cuisine grossiers présentant un risque important pour la sécurité. Une image que les partisans du génie génétique ont paradoxalement tenté de combattre jusqu’à présent. Cette image provoque un certain sentiment de déjà-vu chez les détracteurs du génie génétique : lors de la découverte de CRISPR/Cas9, le génie génétique classique, jusqu’alors considéré comme polyvalent, a rapidement été qualifié de grossier et peu fiable.
Mais sur quelles propriétés du nouvel outil « Prime Editing » ces éloges se basent-ils ? Et en quoi cette nouvelle méthode est-elle meilleure que l’instrument standard actuel, CRISPR/Cas9 ?
L’un des inconvénients des ciseaux génétiques CRISPR/Cas9 est qu’ils coupent les deux brins d’ADN et laissent la cellule réparer de manière incontrôlée les dommages causés. Une rupture double brin dans une cellule est en effet une erreur fatale, c’est pourquoi le mécanisme de réparation automatique de la cellule est immédiatement déclenché. Cependant, celui-ci est très imprécis et insère au hasard dans la zone ouverte des fragments d’ADN présents qui ont été introduits dans la cellule avec les ciseaux génétiques comme modèle. Outre les modifications souhaitées, cela entraîne souvent des mutations indésirables, c’est pourquoi cette méthode est particulièrement adaptée à la désactivation de certains gènes.
Le Prime Editing devrait désormais permettre de contourner en grande partie ce processus de réparation. Pour ce faire, on utilise une enzyme de coupure modifiée qui ne coupe qu’un des deux brins. Comme il n’y a pas de rupture du double brin, le système de réparation cellulaire, sujet aux erreurs, n’est pas activé. Cela permet un meilleur contrôle de l’édition, qui n’est plus laissée au hasard.
Le Prime Editing n’est certes pas la première méthode qui ne provoque pas de rupture du double brin et offre ainsi une précision accrue. Les approches précédentes (par exemple les éditeurs de bases développés par le même groupe de recherche) n’ont toutefois pu être utilisées que de manière limitée jusqu’à présent. Elles permettaient certes de modifier de manière ciblée des lettres individuelles de l’ADN et de corriger ainsi d’éventuelles erreurs conduisant à des maladies, mais elles ne pouvaient pas transformer à volonté toutes les lettres du code génétique en d’autres. Le remplacement n’était possible qu’entre des éléments apparentés (appelés composants complémentaires), par exemple entre la guanine et la cytosine ou entre l’adénine et la thymine. Le Prime Editing devrait désormais permettre de remplacer à volonté chacun des quatre composants de l’ADN par un autre.
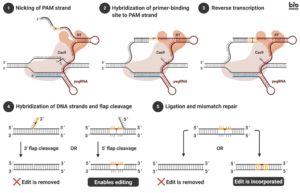
Comment fonctionne le Prime Editing ?
Afin de pouvoir contrôler la coupure avec plus de précision, la molécule qui trouve la zone cible de l’enzyme de coupure sur l’ADN (ADN guide) et la protéine de coupure elle-même ont été modifiées.
Contrairement à CRISPR/Cas9, dans le Prime Editing, le modèle pour la nouvelle information génétique n’est plus introduit dans la cellule sous forme de fragments d’ADN. Il est plutôt intégré dans la molécule d’ARN guide. Ainsi, celle-ci non seulement reconnaît l’endroit à couper dans le génome et y guide l’enzyme de coupe Cas9, mais sert également de modèle pour la modification prévue. Afin de pouvoir traduire ce modèle d’ARN en ADN, la protéine de coupe Cas9 a dû être associée à une autre enzyme (appelée transcriptase inverse) capable de transcrire des séquences d’ARN en ADN. Le processus est alors relativement simple : lorsque l’ARN guide trouve la séquence cible, les ciseaux génétiques modifiés coupent un brin d’ADN. La transcriptase inverse intégrée dans les ciseaux génétiques traduit la nouvelle information génétique fournie dans l’ARN guide en ADN. Celle-ci est intégrée dans le génome de l’organisme cible, tandis que la séquence d’ADN d’origine est reconnue comme superflue par une enzyme de coupure propre à la cellule et coupée. Cependant, comme les deux brins d’ADN présentent désormais deux séquences non correspondantes, le complexe enzymatique de coupure est guidé par un autre ARN guide vers l’emplacement correspondant du brin d’ADN jusqu’alors inchangé et le coupe. C’est seulement à ce moment-là que les mécanismes de réparation propres à la cellule sont utilisés, qui utilisent la séquence ajoutée artificiellement comme modèle et, à partir de celle-ci, produisent la séquence de bases complémentaire sur le brin opposé.
Ce procédé permet un meilleur contrôle du processus de transformation et vise à réduire le nombre d’effets indésirables non ciblés (off-targets). Ces derniers ne devraient plus concerner qu’un dixième des cellules modifiées, alors que 90 % des cellules étaient touchées avec CRISPR/Cas.
Risques non encore testés
Mais une réduction des risques ne signifie pas qu’ils sont inexistants. Le Prime Editing n’est exempt ni de risques, ni de mutations indésirables. Les gènes faisant partie d’un réseau plus vaste dont les éléments interagissent entre eux, ce n’est qu’une question de temps avant que les premiers problèmes liés à cette méthode n’apparaissent et qu’elle ne soit elle aussi discréditée comme une « hache dans la forêt génétique ». Comme le soulignent ses inventeurs eux-mêmes, afin de pouvoir évaluer les conséquences de l’intervention, il faut rechercher des modifications indésirables dans l’ensemble du génome. Jusqu’à présent, cette nouvelle technique a été testée sur quelques types de cellules humaines et sur des cellules nerveuses de souris. On ne sait pas encore si et dans quelle mesure ces nouvelles ciseaux génétiques fonctionneraient dans d’autres types de cellules, c’est-à-dire « in vivo ». Ce nouvel outil n’est donc pas encore prêt à être utilisé sur des patients.
Mais il pourrait rapidement gagner en popularité dans le domaine de la recherche. On spécule déjà sur son utilisation dans la culture des plantes. Le problème reste le même que pour les autres outils d’édition génomique, à savoir une évaluation insuffisante des risques liés aux effets secondaires indésirables de la modification génétique. Ceux-ci peuvent résulter non seulement de la nouvelle méthode, mais aussi, comme pour toutes les autres interventions génétiques précédentes, de l’introduction du nouveau matériel génétique ou de la culture ultérieure des plantes.
Il serait donc prématuré et irresponsable d’utiliser cette précision améliorée comme argument pour renforcer le lobbying contre une réglementation stricte du génie génétique dans l’agriculture.
Sur le plan commercial, le Prime Editing semble offrir un énorme potentiel, ce qui pourrait également le rendre attrayant pour l’industrie agricole. Prime Medicine, une entreprise cofondée par David Liu, le découvreur de la méthode, est titulaire d’une licence pour les applications testées par le groupe de recherche. Si l’utilisation non commerciale et la poursuite des recherches sur cette approche sont autorisées, les demandes commerciales pour le système en instance de brevet pourraient s’avérer coûteuses.
Service d’information sur le génie génétique concernant le Prime Editing


